急性髓系白血病(AML)是最常见的血液系统肿瘤性疾病之一,其发病中位年龄为67岁,现发病越来越老年化,75岁以上的AML患者更常见。老年AML患者在化疗后会出现严重的不良反应以及脏器储备功能和免疫应答降低,从而导致缓解效果不佳,生存期缩短。
移植是AML患者重要的治疗手段之一,但老年患者因年龄较大、体能状态差、合并症多,因此对于此类患者,如何安全地提高移植治疗效果,改善生存质量并延长生存期是血液科医生需要攻克的难题。通过一例病例进行分享。
病例分享
患者基础情况
老年女性患者,68岁
2018年10月因三系减少就诊,骨髓形态学:有核细胞增生活跃,原始细胞28%,化学染色:POX(+)NSE(-)NAF抑制(-),红系有病态造血,可见核出芽、嗜碱性点彩幼红细胞,巨核细胞全片17个,提示AML-M2。
免疫分型:52%原幼细胞,表达CD34,CD33,CD117
细胞遗传学:正常核型46XX[5]
分子生物学:融合基因隐形,WT1基因高表达:50.18%
治疗经过
初始治疗:
2018.10诱导治疗:地西他滨+米托蒽醌+阿糖胞苷+C-CSF一个疗程,达到完全缓解(CR)。
2018.12巩固治疗:HD-ARA-C2gq12h×3d一个疗程。
2019.1;2019.4;2019.5;2019.7先后4程HHA+ARA-C方案化疗巩固后休疗。
疾病复发:
2020.3三系再次降低,×109/L,Hb90g/L,Plt69×109/L,入高博医学(血液病)上海研究中心上海闸新医院。
骨髓形态学:有核细胞增生活跃,原始细胞28.6%,化学染色:POX(+)NSE(-)NAF抑制(-),红系见轻度巨幼样变,巨核细胞全片41个,提示AML-M2可能。
免疫分型:20.57%原幼细胞,表达CD38、CD33、CD117,部分表达CD34。
细胞遗传学:正常核型46XX[10]。
分子生物学:融合基因MLL-PTD高表达30.65%,WT1基因高表达:65.42%
复发后治疗:
2020.3.17再次诱导治疗:地西他滨+伊达比星×1疗程,达到部分缓解(PR),骨髓形态学原始细胞9.2%。
建议行Allo-HSCT,患者以及家属表示年龄接近70岁,顾虑大。
后患者及家属经过反复权衡,决定行Allo-HSCT,供者为女儿41岁,HLA5/10,DSA:弱阳性,血型为A供A,体检合格。
患者移植前合并症指数1分(肺部感染),ECOG1分。
移植:
考虑到患者的基本情况,团队采取了减低强度的预处理方案,患者移植过程比较顺利,包括心脏、肝肾等各方面脏器功能都能耐受治疗。
移植过程中出现了感染的症状,但主要是口腔黏膜炎,未出现严重的胃肠道症状。中性粒细胞在12天时植入,巨核系细胞植入时间为14天,基本上从移植后到末次随访都呈安全嵌合的状态,即嵌合率99%以上。
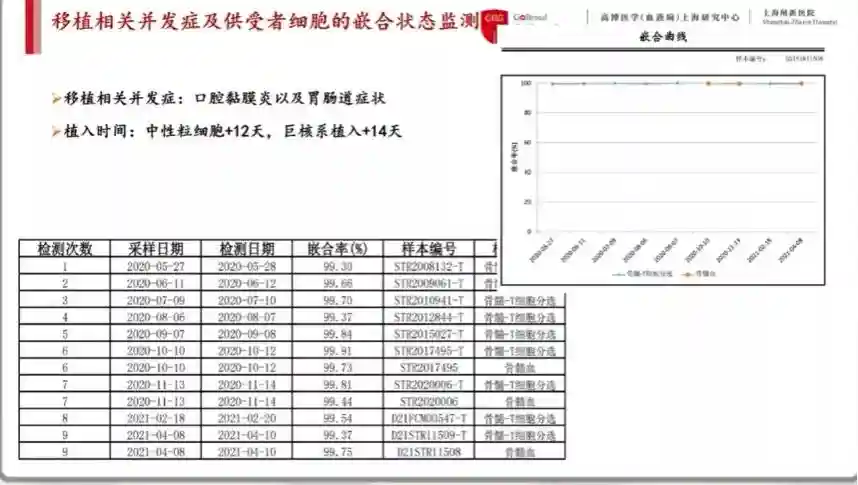
图1移植相关嵌合状态检测
移植后原发病微小残存病灶(MRD)检测结果显示处于低水平状态。
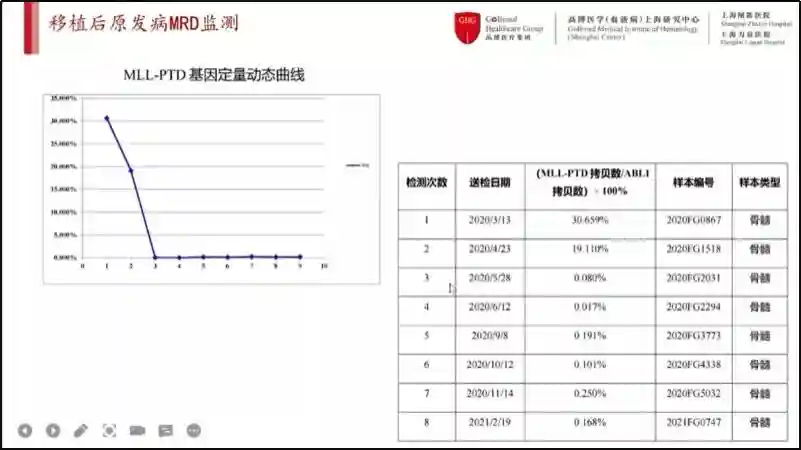
图2MRD监测
基于嵌合度动态监测以及MRD检测,对该患者的免疫抑制剂进行了如下调整:

图3免疫抑制剂调整
该患者移植后完全嵌合且MRD低表达,同时无急性移植物抗宿主病发生;该患者随访到现在已超过一年,且依旧保持着无病生存的状态,各方面情况良好。
老年AML患者如何进行Allo-HSCT?
听听国内外文献怎么说
老年AML患者合并症多,治疗难度大,预后差,有学者统计老年AML患者CR率仅为40%,生存期约为6-10个月,2年生存率约为15%。随着减低强度预处理方案的应用、支持治疗的进展,越来越多的老年患者接受了Allo-HSCT。
欧美国家接受Allo-HSCT的患者中,老年患者占22%,年龄也已经突破到70岁以上。但是我国接受Allo-HSCT的老年AML患者并不高,仅为6%左右。
Allo-HSCT是老年AML首次缓解后的最佳治疗方法吗?既往有研究显示:能够接受Allo-HSCT的患者总生存(OS)远远高于没有接受Allo-HSCT的患者,Allo-HSCT能为将近50%的老年AML患者带来生存获益。
另一项研究回顾了向国际血液和骨髓移植研究中心(CIBMTR)报告的1080名接受减低强度预处理移植患者的数据。单变量分析显示非复发死亡(NRM)、2-4级急性GVHD、慢性GVHD、复发、无疾病生存(DFS)、OS等无年龄组差异。
多变量分析显示年龄对NRM、复发、DFS或OS无显著影响。HLA匹配差异程度对2年NRM、DFS和OS产生不利影响,预后不良的细胞遗传学对复发、DFS、OS产生不利影响,更好的HCT体前状态预示着2年OS的改善,因此老年患者不应该视为HCT的禁忌症。
谈及Allo-HSCT的年龄上限时,欧洲血液和骨髓移植学会(EBMT)比较了2004年至2014年间713名70岁以上AML患者和16161名50-69岁接受HSCT患者的结果:急性和慢性GVHD在两个年龄组中无统计学差异,老年患者的TRM较高,总体2年生存率较低,但70岁并不是一个不可逾越的障碍。
既往研究显示:年龄在55岁及55岁以上,移植匹配无关供者(MUD,中位年龄35岁)或HLA相同的匹配同胞供体(MSD,中位年龄61岁),3年TRM、复发率和OS均无显著差异,提示老年患者的年长同胞适合为患者提供造血干细胞。
在明尼苏达州的一项前瞻性研究中,98名年龄在55岁及55岁以上接受减低强度预处理(RIC)方案HSCT的AML患者使用匹配的同胞供体或脐血,同胞供体组有26例,脐血组有44例;OS、复发率和TRM无差异;36名脐带血HSCT受者在移植后2年内的慢性GVHD发病率较低。
GVHD、感染、预处理方案的毒性以及共病的恶化都会导致移植相关死亡率(TRM),这是反对老年Allo-HSCT的论点,但在过去几十年中,AML患者TRM已经显著降低,但老年依然是TRM的预测因素,尤其是伴GVHD的老年患者。
关于降低TRM的措施,可以考虑减少化疗疗程的数量:德国学者的一项AML研究中,接受两个疗程化疗后立即行同种异体HSCT的患者生存率最佳。同时老年AML患者先进行一个疗程的诱导化疗然后进行Allo-HSCT的临床研究正在进行中。
疾病状态、医学共病、体能状态等似乎更可以预测预后,年龄不应作为老年AML患者接受Allo-HSCT的独立限制条件。
移植风险评估系统有:HCT-CI、EBMT积分体系、ECOG评分、KPS评分等均有助于预测Allo-HSCT的OS、TRM、NRM等。老年综合评估(CGA)是依据生物-心理-社会-环境的医学模式,对老年患者的疾病、体能、情感、认知、心理、社会和经济等做出多维度多参数综合评价,相对传统的评估,能够发现更多问题,让多学科团队早期干预。
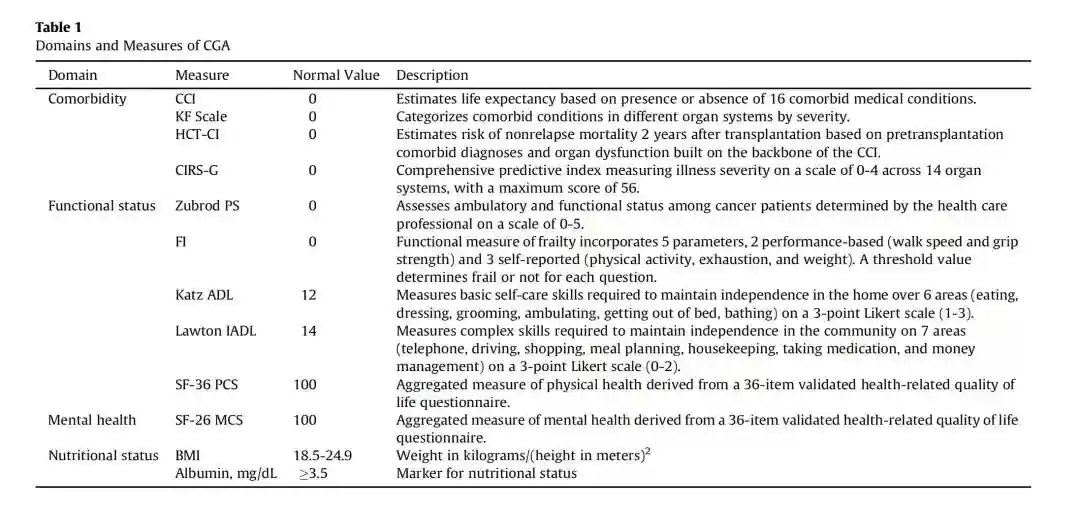
图4CGA评估系统条目
老年Allo-HSCT预处理方案的选择上多用减低剂量预处理(RIC)方案,即以氟达拉滨为基础的化疗,联合或不联合全身放疗(TBI),化疗剂量和/或放疗剂量至少减少30%,但RIC方案的不足之处是复发率较高,清髓性(MAC)方案虽能降低复发率,但随着TRM的增加,并不能给患者带来生存获益。
王椿教授团队采取BU+ARA-C+TBI+FLU为基础的预处理方案,加入TBI进行免疫清除,避免了细胞毒药物对重要脏器的损伤,使老年患者获益。
急性和慢性GVHD仍然是HSCT成功的主要障碍,老年患者更是如此,近年来PT-Cy引入GVHD预防,使半相和移植GVHD的发生率和致死率得到明显降低,同时也使老年移植患者获益。
“北京方案”单倍型移植中将ATG引入预处理方案,无论是单中心还是多中心、回顾性还是前瞻性研究的结果均表明:不同年龄移植患者的GVHD发生率没有差异。
因此,老年不应该被视为HSCT的障碍和禁忌;移植前老年健康状态的多维度评估是确定老年移植方案决策的重要前提;随着临床移植经验积累及移植技术的不断改进,老年移植预后、生活质量正在得到改善。
专家介绍:朱骏

高博医学(血液病)上海研究中心医疗总监副主任医师
曾就职于上海市第一人民医院血液科,拥有20年专业血液病诊治诊疗经验。临床及科研主攻方向是造血干细胞移植治疗难治性血液病,粒缺伴发热患者感染预防和治疗等,负责相关领域多中心的临床研究,并在知名杂志上发布论文。
擅长:各类血液病的诊断和治疗,如血友病、各类贫血、血小板减少、白细胞减少、骨髓增殖性疾病、急慢性白血病、恶性淋巴瘤、多发性骨髓瘤、再生障碍性贫血,骨髓增生异常综合征。
编辑|大福
审核|朱骏