单倍体胚胎干细胞的建立为遗传筛选研究、制备基因编辑动物模型提供了新的手段,是极具价值的遗传学研究工具。然而,其在日常培养和分化过程中,常常发生的二倍化现象,严重影响其发挥“基因筛选利器”的功能。如何抑制二倍化,高效获得单倍体胚胎干细胞成为干细胞研究界的重要课题。

日前,南开大学药物化学生物学国家重点实验室帅领课题组发现,通过基因调控,抑制细胞凋亡可以减少小鼠单倍体胚胎干细胞在日常培养和分化过程中的二倍化现象。这一发现为获取各种单倍体分化细胞提供了一种快速有效的策略,推广了单倍体细胞在各个谱系的遗传学筛选研究。6月5日,介绍该工作的论文在线发表于国际学术期刊《干细胞报道》。
二倍化使“基因筛选利器”应用于科研受限
据介绍,真核生物的遗传信息一半来自父本,一半来自母本。因此,在自然情况下,细胞中具有两套染色体(即二倍体细胞),这也是哺乳动物传递遗传信息的方式,并通过减数分裂来抵御环境变迁,保障物种繁衍。但是,对于遗传学研究,尤其是隐性遗传基因功能的探索,二倍体细胞往往由于存在等位基因而受限。

正是由于单倍体干细胞具有纯合子表型和干细胞多分化潜能等特征,因此,可以快速地将其应用于探索新颖基因的未知功能。然而,这一类人造纯合子的工具细胞,在日常培养或分化路径中,倾向于自发二倍化,进而丧失了单拷贝基因组的优势。因此需要依靠费时而复杂的分选方式去周期性的富集单倍体细胞,从而大大局限了单倍体干细胞在多个领域的应用。
2019年Jiye等运用GeCKO人类全基因组CRISPR/Cas9敲除文库筛选技术,研究者在多发性骨髓瘤细胞中鉴定出了咪唑药物已知靶点CRBN,另外还筛选到了CNS9信号转导体中的7个蛋白,并通过进一步研究发现CSN9信号体功能的丧失激活了scfbxo7复合物,增强了CRBN的降解,从而赋予了细胞咪唑抗性。
2015年,Chen等通过在小鼠动物模型中应用CRISPR技术筛查到了参与肿瘤迁移的基因。首先,他们构建了针对小鼠全基因组的混合sgRNA文库。然后,他们将Cas9-GFP蛋白整合到小鼠非小细胞肺癌细胞系中,形成Cas9-GFP-KPD细胞系,再用sgRNA混合文库侵染。在培养1周之后,文库稳定表达并具有足够的拷贝数与均匀性,然后将该细胞系(mGeCKOa-transduced)与对照组细胞系(Untransduced)各自移植到小鼠体内,并分别对早期肿瘤与晚期肿瘤的样本进行分析。

研究者们发现,经文库侵染的一些细胞最终具有高迁移能力,而对照组细胞系形成的肿瘤均不具有迁移性。利用二代测序技术,研究者们分别鉴定了在肿瘤原位与转移灶处被敲除的基因,这些基因的功能可能是抑制肿瘤生长或迁移。
“因此,探究单倍体干细胞的二倍化机制,从而从根本上有效地维持单倍体干细胞的单倍性,对于推广此类遗传学筛选研究的工具细胞具有深远的意义。”帅领说。
基因调控可维持单倍体干细胞的单倍性
帅领课题组研究发现,敲除基因组中的p53基因可以稳定维持小鼠单倍体胚胎干细胞的单倍性。他们发现,p53敲除的小鼠单倍体干细胞在进行体外分化时,可获得单倍体纯度极高的拟胚体、上胚层干细胞样细胞和神经干细胞样细胞。而体内分化实验证明,p53敲除的小鼠单倍体胚胎干细胞可以通过嵌合体实验贡献到胚胎发育第6.5天、第8.5天和第10.5天,并保持很高的单倍体比例。另外,在畸胎瘤体内分化实验中也能检测到单倍体的体细胞。
为了探究p53敲除的小鼠单倍体胚胎干细胞稳定维持单倍性的原因,研究人员通过转录组测序分析发现,p53敲除的小鼠单倍体胚胎干细胞中,凋亡基因的表达量出现了明显下调,而p53相关的其它信号通路的基因表达水平却没有看见明显的差异。后续结果表明,凋亡基因p73的缺失也可以有效维持小鼠单倍体胚胎干细胞的单倍性。
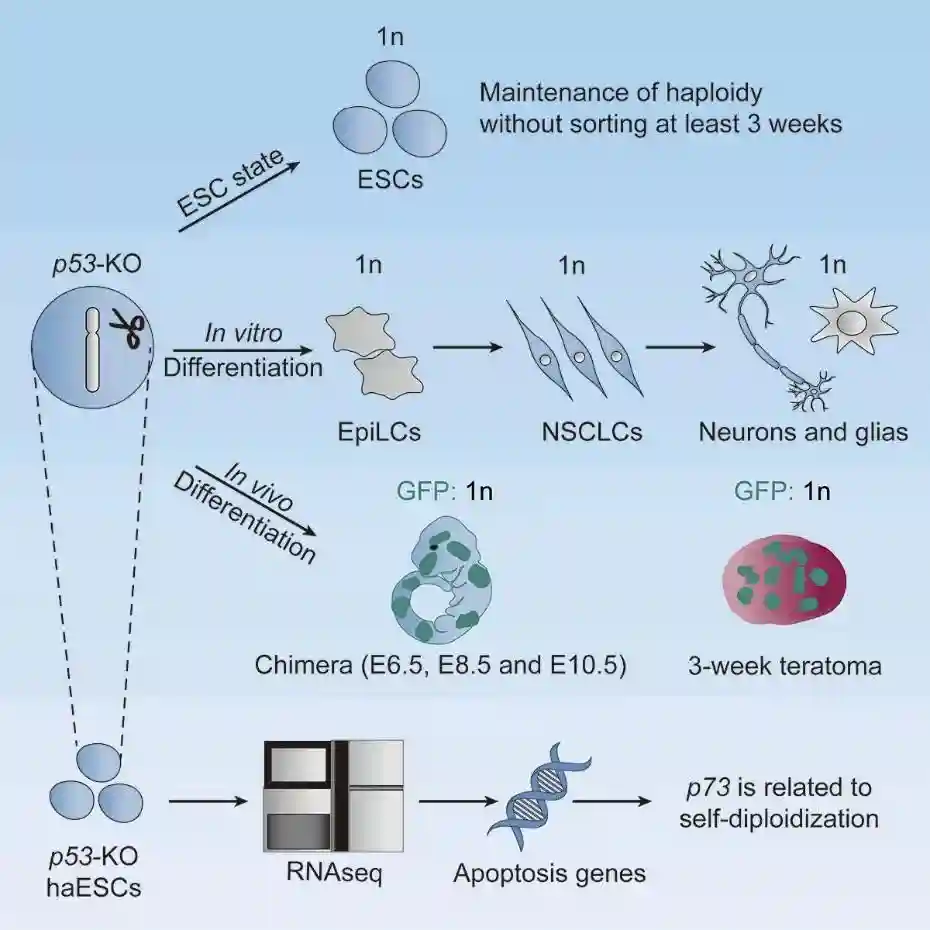
“我们的研究证明了p53敲除主要通过对细胞凋亡的抑制来维持小鼠单倍体胚胎干细胞在日常传代培养和体内外分化过程中的单倍性。这为获取各种单倍体分化细胞提供了一种快速有效的策略,也推广了单倍体细胞在各个谱系的遗传学筛选研究。
蚯蚓为何切两半还能再生?我科学家找到关键基因蚯蚓不仅是土壤生态系统中的重要成员,也以拥有极强的前后部体节再生能力著称。但以前,蚯蚓为何拥有再生的本领一直是个谜。近日,中科院昆明动物研究所发表在《自然·通讯》上的一项研究成果,揭示了蚯蚓再生的分子细胞学机制。
自然界中动物的再生能力,一直是个令人着迷且非常复杂的生物学过程。斑马鱼、蝾螈、壁虎等脊椎动物可以治愈创伤,甚至让丢失的心脏、尾巴、晶状体器官或者附肢再生。用少量组织和细胞再生整个生命体的“本领”,也被广泛用于干细胞生物学和再生医学研究。
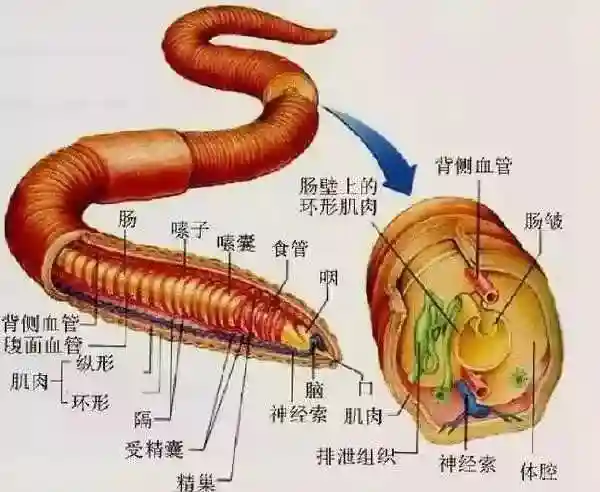
对于蚯蚓,达尔文曾在《腐殖土的形成和蚯蚓的作用》中感叹:“我们很难找到其他的生灵像它们一样,虽看似卑微,却在世界历史的进程中起到了如此重要的作用。”
中科院昆明动物研究所吴东东课题组测序并拼装了准染色体水平的高质量安德爱胜蚓基因组,并通过不同再生时期bulk转录组(批量测序)和单细胞转录组整合揭示蚯蚓再生的分子细胞学机制。研究发现蚯蚓基因组中重复序列LINE2转座元件可能在蚯蚓再生中扮演重要调控角色,例如LINE2转座元件显著高比例地插入到蚯蚓早期再生相关的差异基因位点;同时某些差异表达的LINE2转座元件和它们的邻近基因拥有极为相似的表达模式。
课题组发现,核心调控涡虫这样的高度再生物种的EGR1(一种早期生长因子),不仅在蚯蚓再生过程中发生差异高表达,而且其侧翼的LINE2转座元件也发生显著差异表达上调,因此推测这些显著差异表达的元件可能通过调控邻近基因来参与蚯蚓再生过程。另一方面,课题组在蚯蚓基因组中发现大量基因复制事件,这些扩张的基因家族主要富集在发育生物学通路,而发育和再生在某些通路可能往往是共通的。
课题组还发现,某些显著扩张的基因家族可能通过增加其拷贝数剂量效应来调控蚯蚓再生过程。此外,蚯蚓再生早期的单细胞转录组解析暗示,蚯蚓再生早期72小时后损伤愈合部位细胞的高比例组分是干细胞,且多能干细胞在蚯蚓再生早期过程中具有重要作用。此项研究提供了一些蚯蚓再生的候选分子细胞学机制,提出蚯蚓可作为研究再生生物学或再生医学的新模型。