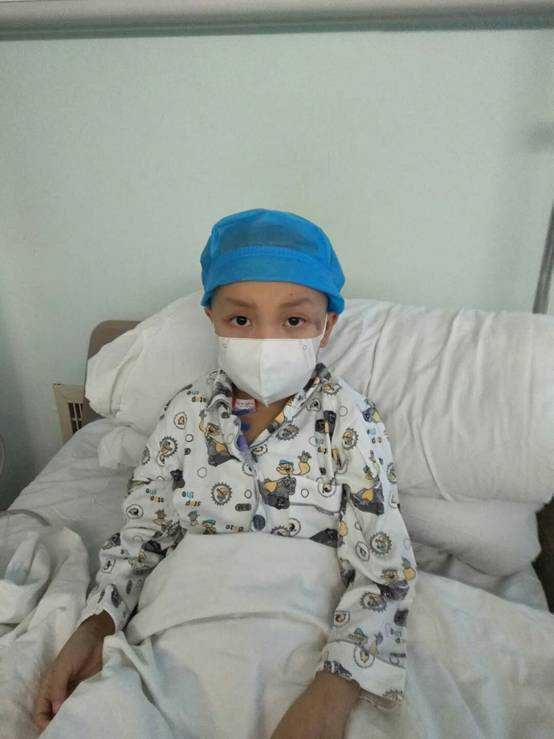
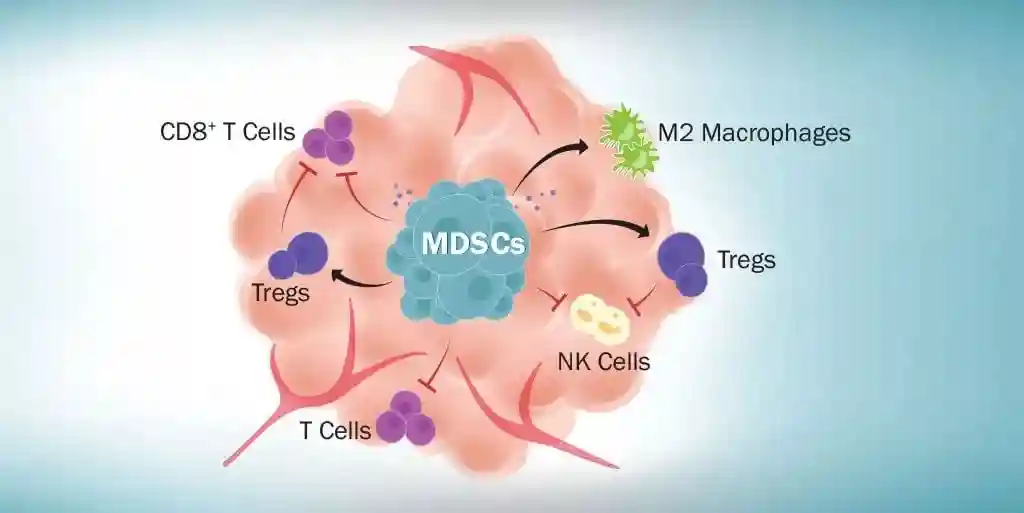
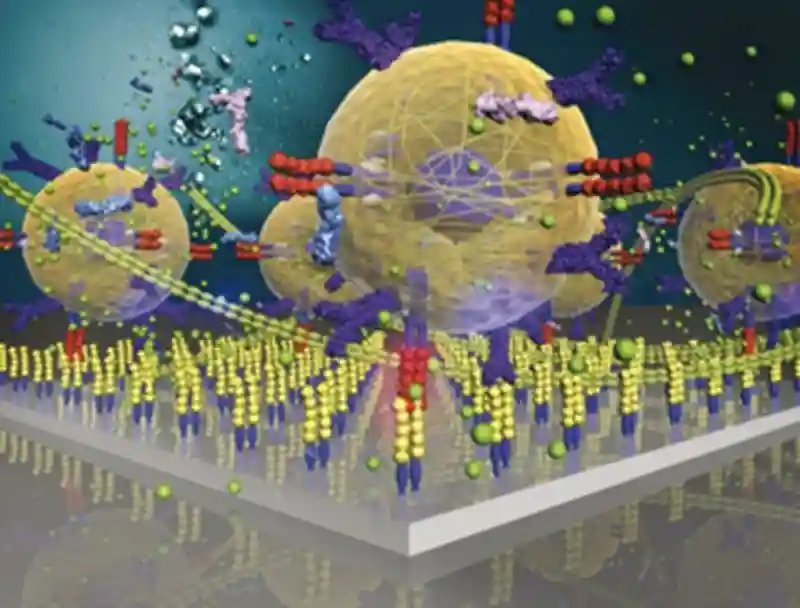
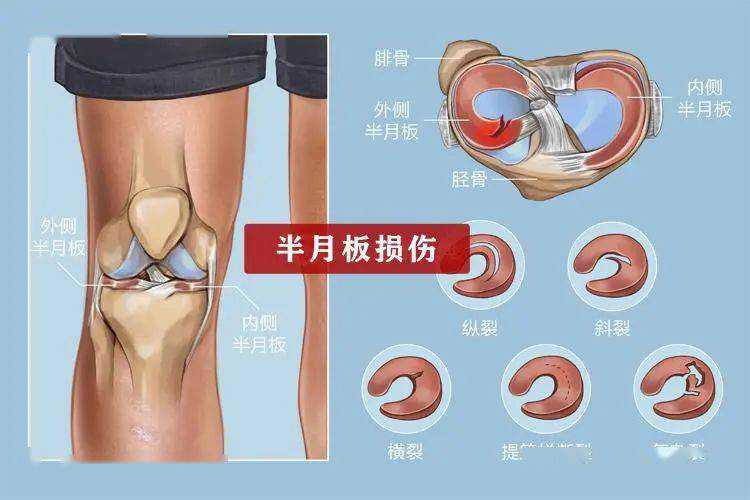
图片说明:大脑海马体中的细胞图像显示,生长因子TGF-beta1(染色为红色)在年轻的组织中几乎不存在,而在衰老的组织中大量出现。TGF-beta1在组织中抑制干细胞再生,并引起炎症和衰老。图片说明:DavidSchafferIrinaConboy,UCBerkeley
无论你是否头脑灵活或肌肉结实,还是二者皆有,有一天你也可能受益于一种能使老化的大脑和肌肉组织年轻化的药物。
加利福尼亚大学(UniversityofCalifornia)的研究人员发现,一种小分子药物能同时激活小鼠大脑和肌肉中的老龄干细胞。这一发现将带来针对人体的药物干预,让整个身体中的老化组织重新变得年轻起来。

该研究的共同作者、加利福尼亚大学干细胞中心(StemCellCenter)主任、化学和生物分子工程教授DavidSchaffer指出:“我们确信,使用单一的小分子就可以挽救老化的大脑组织和肌肉的主要功能。这真是一大福音,因为每个组织中衰老的分子机制都不同,我们不可能使用一种单一的干预方式挽救多个组织的功能。”
这种药物会干预生长因子的活动,转化生长因子β1(TGF-beta1)。过去10年,Schaffer在加州大学伯克利分校(UCBerkeley)的同事IrinaConboy发现,这种因子会抑制多种干细胞更新组织的能力。
生物工程学副教授Conboy说:“根据我们早期的论文来看,TGF-beta1途径似乎是多组织衰老的主要罪魁祸首之一。一种蛋白上调,会使不同器官(例如大脑、胰腺、心脏和肌肉等)中的多种干细胞衰老。这确实是我们首次发现可以使用一种药物使得关键的、促进衰老的TGF-beta1途径显得更年轻,从而修复多个器官系统。”
加州大学伯克利分校的团队将结果发表在2015年5月13日的Oncotarget上。Conboy和Schaffer是一个教师财团的成员,他们在加州定量生物科学研究所(CaliforniaInstituteforQuantitativeBiosciences,QB3)研究衰老。
干细胞受抑制导致衰老
衰老的部分原因在于成体干细胞不能形成代替物来替换受损细胞,从而修复身体组织。研究人员发现,干细胞活性降低主要是由干细胞周围环境中的抑制性化合物引起的。其中部分化合物是由于慢性、低水平炎症(衰老的一个特征),免疫系统将其释放至此。
2005年,Conboy和同事将年幼小鼠的血液灌输进入老年小鼠体内,这个过程称为异种共生,目的在于修复肌肉、肝脏、大脑/海马体中的干细胞,结果显示,年幼小鼠血液中的化学物质竟然能使衰老干细胞周围的化学环境年轻化。2014年,医生进行了小规模试验来确定年轻人的血浆是否能帮助逆转老年阿尔茨海默病患者的大脑损害。
然而,这种治疗即使无害,却也不太可行。因此,Conboy,Schaffer和其他人试图找出一种能安全、持续使用的特异性化合物,用于维持许多器官中干细胞的年轻化环境。一种多组织年轻化的关键化合物靶标是TGF-beta1,它会促使体内所有组织衰老,在高浓度时,Conboy发现其会抑制干细胞的活性。
Schaffer的研究方向为大脑中的神经干细胞,5年前,他与Conboy合作研究TGF-beta1在海马体内的活性。海马体是大脑内对于记忆和学习非常重要的区域,而衰老的标志即学习、认知和记忆的下降。在这项新研究中,他们发现,在老龄小鼠体内,海马体中TGF-beta1的增加与血液和其他衰老组织中相似。
Schaffer将一种病毒载体用于基因治疗研究,研究团队在老龄小鼠体内插入遗传性阻断子下调TGF-beta1的活性,他们发现海马体干细胞表现地更加年轻化,并开始产生新的神经细胞。
药物让衰老组织变得更聪明
接着研究团队向血液中注射了一种能阻断TGF-beta1受体的化合物,从而降低TGF-beta1的作用。Conboy说,这种小分子是一种Alk5激酶抑制剂,它作为一种抗癌药物已经在临床试验。这种小分子成功恢复了老龄程度相同的动物大脑和肌肉组织中干细胞的功能,这可能让这些动物变得更强壮、更聪明。
Conboy说,“这种关键的TGF-beta1调控途径重置到年轻化的信号水平,还使组织炎症减少,因此为干细胞通信促成了更加有利的环境。这样可以同时在完全不同的组织中改善组织修复并维持修复,例如肌肉和脑组织。”
研究人员指出,这仅仅是迈向治疗的第一步,因为其他生物化合物因素同样调节成体干细胞的活性。Schaffer和Conboy的团队正在就一种多管齐下的方法进行合作,这种方法调节两种关键的生物化学调节因子,或许可以安全地恢复多个衰老及病理组织中干细胞的反应。
Conboy说:“摆在我们前面的挑战是使用少量的化合物仔细地调节干细胞环境中的多个信号途径,这样我们才能最终重新使环境年轻化。对于修复干细胞环境,剂量将变得至关重要。”(科学之家,译审:HHLang)